Peptida ialah kelas sebatian yang dibentuk oleh penyambungan pelbagai asid amino melalui ikatan peptida.Mereka ada di mana-mana dalam organisma hidup.Sehingga kini, puluhan ribu peptida telah ditemui dalam organisma hidup.Peptida memainkan peranan penting dalam mengawal selia aktiviti fungsi pelbagai sistem, organ, tisu dan sel dan dalam aktiviti kehidupan, dan sering digunakan dalam analisis fungsi, penyelidikan antibodi, pembangunan ubat dan bidang lain.Dengan perkembangan bioteknologi dan teknologi sintesis peptida, semakin banyak ubat peptida telah dibangunkan dan digunakan di klinik.
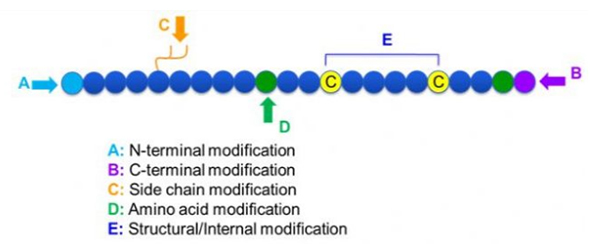
Terdapat pelbagai jenis pengubahsuaian peptida, yang boleh dibahagikan secara ringkas kepada pengubahsuaian pasca dan pengubahsuaian proses (menggunakan pengubahsuaian asid amino terbitan), dan pengubahsuaian N-terminal, pengubahsuaian C-terminal, pengubahsuaian rantai sisi, pengubahsuaian asid amino, pengubahsuaian rangka, dsb., bergantung pada tapak pengubahsuaian (Rajah 1).Sebagai cara penting untuk menukar struktur rantai utama atau kumpulan rantai sampingan rantai peptida, pengubahsuaian peptida secara berkesan boleh mengubah sifat fizikal dan kimia sebatian peptida, meningkatkan keterlarutan air, memanjangkan masa tindakan dalam vivo, menukar pengedaran biologi mereka, menghapuskan imunogenisiti. , mengurangkan kesan sampingan toksik, dsb. Dalam kertas kerja ini, beberapa strategi pengubahsuaian peptida utama dan ciri-cirinya diperkenalkan.
1. Kitaran
Peptida kitaran mempunyai banyak aplikasi dalam bioperubatan, dan banyak peptida semula jadi dengan aktiviti biologi adalah peptida kitaran.Oleh kerana peptida kitaran cenderung lebih tegar daripada peptida linear, ia sangat tahan terhadap sistem pencernaan, boleh bertahan dalam saluran pencernaan, dan mempamerkan pertalian yang lebih kuat untuk reseptor sasaran.Kitaran ialah cara paling langsung untuk mensintesis peptida kitaran, terutamanya untuk peptida dengan rangka struktur yang besar.Mengikut mod kitaran, ia boleh dibahagikan kepada jenis rantai sisi sisi, terminal - jenis rantai sisi, terminal - jenis terminal (jenis hujung ke hujung).
(1) rantai sisi ke rantai sisi
Jenis kitaran rantai sisi ke rantai sisi yang paling biasa ialah penghubung disulfida antara sisa sistein.Siklisasi ini diperkenalkan oleh sepasang sisa sistein yang dinyahlindungi dan kemudian dioksidakan untuk membentuk ikatan disulfida.Sintesis polisiklik boleh dicapai dengan penyingkiran terpilih kumpulan perlindungan sulfhidril.Kitaran boleh dilakukan sama ada dalam pelarut selepas pemisahan atau pada resin pra-penyisihan.Kitaran pada resin mungkin kurang berkesan daripada kitaran pelarut kerana peptida pada resin tidak mudah membentuk konformasi berkitar.Satu lagi jenis kitaran rantai sisi - rantai sisi ialah pembentukan struktur amida antara asid aspartik atau residu asid glutamat dan asid amino bes, yang memerlukan kumpulan perlindungan rantai sisi mesti boleh disingkirkan secara selektif daripada polipeptida sama ada. pada resin atau selepas disosiasi.Jenis ketiga rantaian sisi - kitaran rantai sisi ialah pembentukan eter difenil oleh tirosin atau p-hidroksifenilglisin.Jenis kitaran dalam produk semula jadi ini hanya terdapat dalam produk mikrob, dan produk kitaran selalunya mempunyai potensi nilai perubatan.Penyediaan sebatian ini memerlukan keadaan tindak balas yang unik, jadi ia tidak sering digunakan dalam sintesis peptida konvensional.
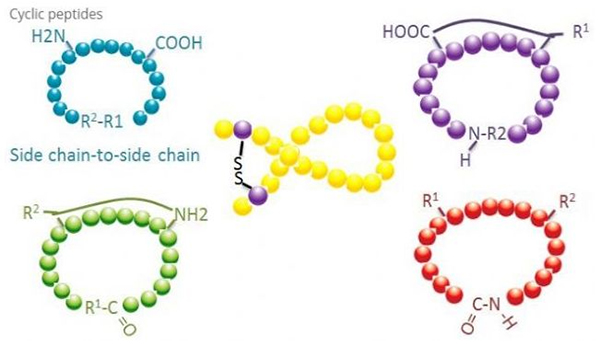
(2) terminal-ke-sidechain
Kitaran rantai sisi terminal biasanya melibatkan terminal C dengan kumpulan amino rantai sisi lisin atau ornithine, atau terminal N dengan rantai sampingan asid aspartik atau asid glutamat.Siklisasi polipeptida lain dibuat dengan membentuk ikatan eter antara terminal C dan rantai sisi serin atau threonine.
(3) Jenis terminal atau kepala-ke-ekor
Polipeptida rantai boleh sama ada dikitar dalam pelarut atau tetap pada resin dengan kitaran rantai sampingan.Kepekatan peptida yang rendah harus digunakan dalam pemusatan pelarut untuk mengelakkan oligomerisasi peptida.Hasil polipeptida gelang sintetik kepala ke ekor bergantung pada jujukan polipeptida rantai.Oleh itu, sebelum menyediakan peptida kitaran secara besar-besaran, perpustakaan kemungkinan peptida plumbum berantai harus dibuat terlebih dahulu, diikuti dengan kitaran untuk mencari urutan dengan hasil terbaik.
2. N-metilasi
N-metilasi pada asalnya berlaku dalam peptida semula jadi dan diperkenalkan ke dalam sintesis peptida untuk menghalang pembentukan ikatan hidrogen, dengan itu menjadikan peptida lebih tahan terhadap biodegradasi dan pelepasan.Sintesis peptida menggunakan derivatif asid amino N-metilasi adalah kaedah yang paling penting.Di samping itu, tindak balas Mitsunobu perantaraan polipeptida-resin N-(2-nitrobenzene sulfonyl chloride) dengan metanol juga boleh digunakan.Kaedah ini telah digunakan untuk menyediakan perpustakaan peptida kitaran yang mengandungi asid amino N-metilasi.
3. Fosforilasi
Fosforilasi adalah salah satu pengubahsuaian pasca terjemahan yang paling biasa dalam alam semula jadi.Dalam sel manusia, lebih daripada 30% protein terfosforilasi.Fosforilasi, terutamanya fosforilasi boleh balik, memainkan peranan penting dalam mengawal banyak proses selular, seperti transduksi isyarat, ekspresi gen, kitaran sel dan peraturan sitoskeleton, dan apoptosis.
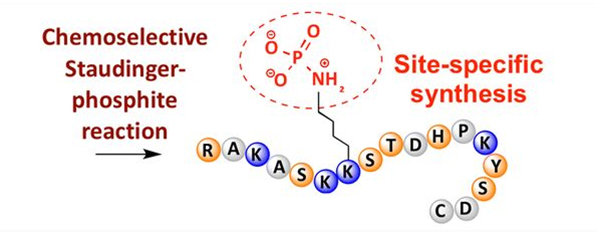
Fosforilasi boleh diperhatikan pada pelbagai sisa asid amino, tetapi sasaran fosforilasi yang paling biasa ialah residu serin, threonine, dan tyrosine.Fosfotirosin, fosfotreonin, dan derivatif fosfoserin boleh sama ada dimasukkan ke dalam peptida semasa sintesis atau terbentuk selepas sintesis peptida.Fosforilasi terpilih boleh dicapai menggunakan sisa serin, threonine, dan tyrosine yang secara selektif mengeluarkan kumpulan pelindung.Sesetengah reagen fosforilasi juga boleh memperkenalkan kumpulan asid fosforik ke dalam polipeptida melalui pengubahsuaian pasca.Dalam tahun-tahun kebelakangan ini, fosforilasi khusus tapak bagi lisin telah dicapai menggunakan tindak balas Staudinger-phosphite terpilih secara kimia (Rajah 3).
4. Myristoylation dan palmitoylation
Asilasi terminal-N dengan asid lemak membolehkan peptida atau protein untuk mengikat membran sel.Urutan myridamoylated pada terminal N membolehkan kinase protein keluarga Src dan protein Gaq transkripase terbalik disasarkan untuk mengikat membran sel.Asid myristic telah dikaitkan dengan terminal N resin-polipeptida menggunakan tindak balas gandingan standard, dan lipopeptida yang terhasil boleh dipisahkan di bawah keadaan standard dan disucikan oleh RP-HPLC.
5. Glikosilasi
Glikopeptida seperti vankomisin dan teikolanin adalah antibiotik penting untuk rawatan jangkitan bakteria yang tahan dadah, dan glikopeptida lain sering digunakan untuk merangsang sistem imun.Di samping itu, oleh kerana banyak antigen mikrob terglikosilasi, adalah sangat penting untuk mengkaji glikopeptida untuk meningkatkan kesan terapeutik jangkitan.Sebaliknya, didapati bahawa protein pada membran sel sel tumor menunjukkan glikosilasi yang tidak normal, yang menjadikan glikopeptida memainkan peranan penting dalam penyelidikan pertahanan imun kanser dan tumor.Glikopeptida disediakan dengan kaedah Fmoc/t-Bu.Sisa glikosilasi, seperti threonine dan serine, sering dimasukkan ke dalam polipeptida oleh fMOC diaktifkan ester pentafluorophenol untuk melindungi asid amino terglikosilasi.
6. Isoprena
Isopentadienylation berlaku pada residu sistein dalam rantai sampingan berhampiran terminal C.Isoprena protein boleh meningkatkan pertalian membran sel dan membentuk interaksi protein-protein.Protein isopentadienasi termasuk tyrosine phosphatase, GTase kecil, molekul cochaperone, lamina nuklear, dan protein pengikat centromeric.Polipeptida isoprena boleh disediakan menggunakan isoprena pada resin atau dengan memperkenalkan derivatif sistein.
7. Pengubahsuaian polietilena glikol (PEG).
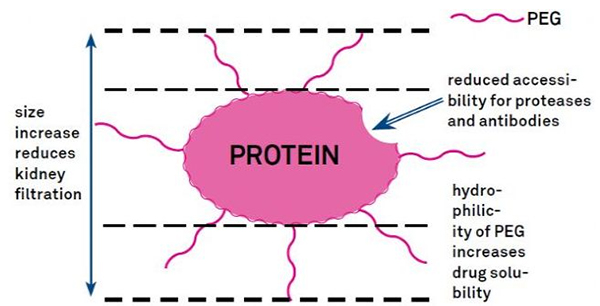
Pengubahsuaian PEG boleh digunakan untuk meningkatkan kestabilan hidrolitik protein, pengagihan bio dan keterlarutan peptida.Pengenalan rantai PEG kepada peptida boleh meningkatkan sifat farmakologinya dan juga menghalang hidrolisis peptida oleh enzim proteolitik.Peptida PEG melalui keratan rentas kapilari glomerulus dengan lebih mudah daripada peptida biasa, sangat mengurangkan pelepasan buah pinggang.Oleh kerana separuh hayat aktif peptida PEG dalam vivo dilanjutkan, tahap rawatan normal boleh dikekalkan dengan dos yang lebih rendah dan ubat peptida yang kurang kerap.Walau bagaimanapun, pengubahsuaian PEG juga mempunyai kesan negatif.Sejumlah besar PEG menghalang enzim daripada merendahkan peptida dan juga mengurangkan pengikatan peptida kepada reseptor sasaran.Tetapi pertalian rendah peptida PEG biasanya diimbangi oleh separuh hayat farmakokinetiknya yang lebih lama, dan dengan berada di dalam badan lebih lama, peptida PEG mempunyai kemungkinan yang lebih besar untuk diserap ke dalam tisu sasaran.Oleh itu, spesifikasi polimer PEG harus dioptimumkan untuk hasil yang optimum.Sebaliknya, peptida PEG terkumpul di dalam hati akibat pengurangan pembersihan buah pinggang, mengakibatkan sindrom makromolekul.Oleh itu, pengubahsuaian PEG perlu direka bentuk dengan lebih teliti apabila peptida digunakan untuk ujian dadah.
Kumpulan pengubahsuaian biasa pengubah PEG boleh diringkaskan secara kasar seperti berikut: Amino (-amine) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimide carbonate - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (seperti propional-ald, butyrALD), asas akrilik (-acrylate-acrl), azido-azide, biotinyl - Biotin, Fluorescein, glutaryl -GA, Acrylate Hydrazide, alkyne-alkyne, p-toluenesulfonate -OTs, succinimide succinate -SS, dll. Derivatif PEG dengan asid karboksilik boleh digandingkan kepada amina terminal-n atau rantai sisi lisin.PEG yang diaktifkan amino boleh digabungkan dengan asid aspartik atau rantai sampingan asid glutamat.PEG teraktif mal boleh dikonjugasikan kepada merkaptan rantai sisi sistein yang tidak dilindungi sepenuhnya [11].Pengubah suai PEG biasanya dikelaskan seperti berikut (nota: mPEG ialah metoksi-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) pengubah PEG rantai lurus
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) pengubah suai PEG dwifungsi
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) pengubah suai PEG bercabang
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinisasi
Biotin boleh terikat kuat dengan avidin atau streptavidin, dan kekuatan pengikatan adalah hampir dengan ikatan kovalen.Peptida berlabel biotin biasanya digunakan dalam immunoassay, histocytochemistry, dan sitometri aliran berasaskan pendarfluor.Antibodi antibiotin berlabel juga boleh digunakan untuk mengikat peptida berbiotinilasi.Label biotin selalunya dilekatkan pada rantai sisi lisin atau terminal N.Asid 6-aminocaproic sering digunakan sebagai ikatan antara peptida dan biotin.Ikatan adalah fleksibel dalam mengikat substrat dan mengikat lebih baik dengan kehadiran halangan sterik.
9. Pelabelan pendarfluor
Pelabelan pendarfluor boleh digunakan untuk mengesan polipeptida dalam sel hidup dan untuk mengkaji enzim dan mekanisme tindakan.Tryptophan (Trp) adalah pendarfluor, jadi ia boleh digunakan untuk pelabelan intrinsik.Spektrum pelepasan triptofan bergantung pada persekitaran persisian dan berkurangan dengan penurunan kekutuban pelarut, sifat yang berguna untuk mengesan struktur peptida dan pengikatan reseptor.Pendarfluor triptofan boleh dipadamkan oleh asid aspartik terprotonasi dan asid glutamat, yang mungkin mengehadkan penggunaannya.Kumpulan Dansyl klorida (Dansyl) sangat pendarfluor apabila terikat kepada kumpulan amino dan sering digunakan sebagai label pendarfluor untuk asid amino atau protein.
Resonans pendarfluor Penukaran tenaga (FRET) berguna untuk kajian enzim.Apabila FRET digunakan, polipeptida substrat biasanya mengandungi kumpulan pelabelan pendarfluor dan kumpulan pelindapkejutan pendarfluor.Kumpulan pendarfluor berlabel dipadamkan oleh pelindapkejut melalui pemindahan tenaga bukan foton.Apabila peptida dipisahkan daripada enzim berkenaan, kumpulan pelabelan mengeluarkan pendarfluor.
10. Polipeptida sangkar
Peptida sangkar mempunyai kumpulan pelindung yang boleh ditanggalkan secara optik yang melindungi peptida daripada mengikat kepada reseptor.Apabila terdedah kepada sinaran UV, peptida diaktifkan, memulihkan pertaliannya kepada reseptor.Oleh kerana pengaktifan optik ini boleh dikawal mengikut masa, amplitud, atau lokasi, peptida sangkar boleh digunakan untuk mengkaji tindak balas yang berlaku dalam sel.Kumpulan pelindung yang paling biasa digunakan untuk polipeptida sangkar ialah kumpulan 2-nitrobenzyl dan derivatifnya, yang boleh diperkenalkan dalam sintesis peptida melalui derivatif asid amino pelindung.Derivatif asid amino yang telah dibangunkan ialah lisin, sistein, serin, dan tirosin.Derivatif aspartat dan glutamat, walau bagaimanapun, tidak lazimnya digunakan kerana kerentanannya terhadap kitaran semasa sintesis dan penceraian peptida.
11. Peptida poliantigenik (MAP)
Peptida pendek biasanya tidak kebal dan mesti digabungkan dengan protein pembawa untuk menghasilkan antibodi.Peptida poliantigenik (MAP) terdiri daripada berbilang peptida yang serupa yang disambungkan kepada nukleus lisin, yang secara khusus boleh menyatakan imunogen berkeupayaan tinggi dan boleh digunakan untuk menyediakan kuplet protein pembawa peptida.Polipeptida MAP boleh disintesis oleh sintesis fasa pepejal pada resin MAP.Walau bagaimanapun, gandingan yang tidak lengkap mengakibatkan rantai peptida yang hilang atau terputus pada beberapa cawangan dan dengan itu tidak menunjukkan sifat polipeptida MAP asal.Sebagai alternatif, peptida boleh disediakan dan disucikan secara berasingan dan kemudian digabungkan dengan MAP.Urutan peptida yang dilekatkan pada teras peptida ditakrifkan dengan baik dan mudah dicirikan oleh spektrometri jisim.
Kesimpulan
Pengubahsuaian peptida adalah cara penting untuk mereka bentuk peptida.Peptida yang diubah suai secara kimia bukan sahaja dapat mengekalkan aktiviti biologi yang tinggi, tetapi juga berkesan mengelakkan kelemahan imunogenisitas dan ketoksikan.Pada masa yang sama, pengubahsuaian kimia boleh memberikan peptida dengan beberapa sifat baru yang sangat baik.Dalam tahun-tahun kebelakangan ini, kaedah pengaktifan CH untuk pengubahsuaian pasca polipeptida telah dibangunkan dengan cepat, dan banyak hasil penting telah dicapai.
Masa siaran: Mac-20-2023
